| Screening |
Points |
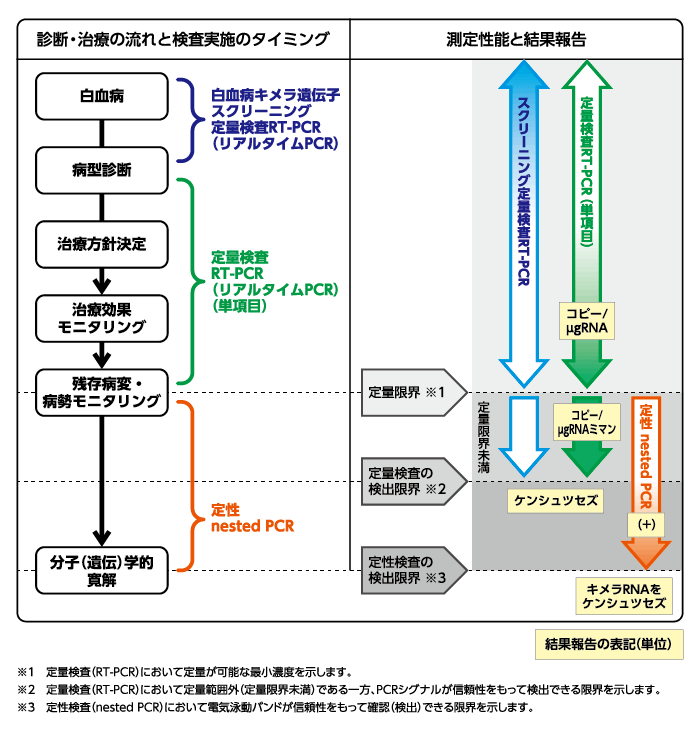
These screenings are used for patients suspected of having leukemia at the initial examination
(at which a high-level expression is seen) to detect leukemia-related chimeric genes.
If chimeric mRNA is detected, the level of the chimeric mRNA is reported as “number of copies/μg RNA.”
For monitoring of treatment, put in a request for each of quantitative and qualitative assays
of the detected chimeric gene at the time of screening.
In the assays, in-house prepared reagents are used. |
| Performance |
The lower limit of quantification (or the lowest reportable value) is 50 copies/μg RNA. |
Parameters
screened |
|
Quantitative assays,
Real-time PCR |
Points |
These assays are used for monitoring of treatment.
Results are reported as “corrected value of chimeric mRNA (number of copies/μg RNA),”
“measured value of chimeric mRNA (number of copies/μg RNA),”
and “measured value of GAPDH (internal standard) (number of copies/μg RNA).”
Reporting results below the lower limit of quantification
■ < 50 copies/μg RNA
■ None-detected (below the detection limit of the assay)
Even if a result is reported as “None-detected (below the detection limit of the assay),”
it does not rule out the possibility of existence of various chimeric genes. Diagnosis shall be
made comprehensively, taking into account other test results and clinical findings.
In the assays, in-house prepared reagents are used. |
| Performance |
The lower limit of quantification (or the lowest reportable value) is 50 copies/μg RNA. |
Parameters
screened |
-
- 02646 2
2646 1
Major BCR::ABL1 mRNA quantitative
- 02984 7
2984 0
minor BCR::ABL1 mRNA quantitative
- 02946 9
2946 2
TCF3::PBX1 mRNA quantitative
- 02989 2
2989 6
PML::RARA mRNA quantitative
- 02988 3
2988 9
CBFB::MYH11 mRNA quantitative
- 02991 9
2991 3
RUNX1::RUNX1T1 mRNA quantitative
- 02993 7
2993 8
ETV6::RUNX1 mRNA quantitative
-
- 02944 1
2944 8
KMT2A::AFF1 mRNA quantitative
- 06835 8
6835 3
KMT2A::AFDN mRNA quantitative
- 02945 0
2945 5
KMT2A::MLLT3 mRNA quantitative
- 06832 1
6832 1
KMT2A::MLLT1 mRNA quantitative
- 02994 6
2994 5
NUP98::HOXA9 mRNA quantitative
- 06830 3
6830 7
STIL::TAL1 mRNA quantitative
- 02992 8
2992 1
DEK::NUP214 mRNA quantitative
|
Qualitative assays,
Nested PCR |
Points |
These assays are used for monitoring of treatment and relapse with high sensitivity to detect
various chimeric mRNAs.
Results are reported as “The chimeric mRNA was none-detected” or “Detected.”
* Qualitative assays also have the detection limit; therefore, a result of “None-detected” does
not completely rule out the possibility of minimal residual disease (MRD).
In the assays, in-house prepared reagents are used. |
| Performance |
The lower limit of detection is 10 copies/μg RNA. |
Parameters
screened |
-
- 06324 5
6324 2
Major BCR::ABL1 mRNA qualitative
- 06325 4
6325 0
minor BCR::ABL1 mRNA qualitative
- 00B92 8
0B92 8
micro BCR::ABL1 mRNA qualitative
- 02498 7
2498 6
TCF3::PBX1 mRNA qualitative
- 06321 8
6321 1
PML::RARA mRNA qualitative
- 02734 4
2734 5
CBFB::MYH11 mRNA qualitative
- 06010 3
6010 7
RUNX1::RUNX1T1 mRNA qualitative
-
- 06016 7
6016 1
RUNX1::MECOM mRNA qualitative
- 02307 8
2307 6
ETV6::RUNX1 mRNA qualitative
- 02293 4
2293 2
KMT2A::AFF1 mRNA qualitative
- 0M498 7
M498 9
KMT2A::AFDN mRNA qualitative
- 02294 3
2294 0
KMT2A::MLLT3 mRNA qualitative
- 02295 2
2295 7
KMT2A::MLLT1 mRNA qualitative
- 06039 2
6039 3
DEK::NUP214 mRNA qualitative
|